babyweb.sk > Chcem dieťa > Umelé oplodnenie > Liečba mužskej neplodnosti
Liečba mužskej neplodnosti
V európskych krajinách stúpa počet infertilných, teda neplodných párov. Zlepšujú sa diagnostické možnosti a zhoršujú sa funkčné parametre spermatozoidu.
Podľa posledných výskumov má zdravé a funkčné spermie, teda normospermie, menej než štyridsaťosem percent mužov vo veku do tridsiatich siedmich rokov. U starších mužov je to pravdepodobne ešte horšie. Problémy s plodnosťou sa týkajú desiatich až pätnástich percent párov. Výskumy potvrdzujú, že u viac než polovice neplodných párov je závažnejší problém na strane muža.
Väčšina problémov sa dá účinne riešiť
Súčasné možnosti diagnostiky, liečby a asistovanej reprodukcie poskytujú šancu stať sa otcami aj mužom, ktorí by pred dvadsiatimi rokmi biologicky nezvládli mať svoje vlastné dieťa.
Vo veľkom množstve informácií, ktoré sú dnes k dispozícii, sa ťažko orientuje už i lekár, nieto ešte pacient, veriaci, že moderné technológie prekonajú všetky prekážky. Informácie, že každý problém sa dá u každého pacienta vyriešiť k jeho úplnej spokojnosti, rýchlo, s úspechom a bez veľkých nákladov, vyvolávajú niekedy mylný pocit všemohúcnosti medicíny. Väčšina problémov sa však vyriešiť dá.
Problémami mužskej neplodnosti sa zaoberá medicínska špecializácia andrológia.
Cieľom andrologickej starostlivosti je stanovenie účinného postupu v niekoľkých nadväzujúcich krokoch:
Diagnostika (vyšetrenie) smerujúca k odpovedi na otázky:
- Ide o riešiteľný stav v zmysle obnovenia prirodzenej plodnosti alebo nie?
- Aké následky má postihnutie pre organizmus muža okrem neplodnosti?
- Ak nie je možné dosiahnuť oplodnenie prirodzenou cestou, aký postup asistovanej reprodukcie má najväčšiu šancu na úspech?
Vo vzťahu k asistovanej reprodukcii sú podstatné tieto veci:
- predpoveď úspechu asistovanej reprodukcie z hľadiska mužského faktora infertility
- zhodnotenie možností prenosu defektu na deti
- príprava muža na asistovanú reprodukciu s cieľom zvýšiť pravdepodobnosť úspechu asistovanej reprodukcie
Andrologická predikcia (predpoveď)
Významnú prediktívnu hodnotu poskytuje základné spermiologické vyšetrenie. Tak, ako je často prezentované (opakovaná azoospermia a oligo-asthenozoospermia) nemá na cieľ predikcie veľký prínos.
Aj rutinne stanovené hodnoty pH, objemu, viskozity a času kolikvácie informujú o funkcii prostatických žliaz a semenných vačkov. Takto je možné získať informáciu o efekte hormonálneho prostredia na prídavné žľazy, ak je súčasne zabezpečený čas sexuálnej karantény pred odberom.
Hodnotenie motility je zvyčajne veľmi orientačné, hodnotenie morfológie často chýba úplne, pričom práve tieto hodnoty výrazne ovplyvňujú schopnosť fertilizácie ova in vitro. Spermiologické vyšetrenie na pracoviskách asistovanej reprodukcie sa často chápe len ako hodnotenie materiálu k prípadnej IVF či IVF-ICSI. Podrobnejšie vyšetrenie je z hľadiska andrológa dôležité najmä u tých párov, ktoré majú za sebou niekoľko embryotransferov a medzi nimi zopár spermiogramov vykonaných v dlhších časových odstupoch.
Spermiogram je funkčné vyšetrenie semenníkov, semenníkových ciest a akcesorných pohlavných žliaz. Má výpovednú hodnotu i z hľadiska predpovede (predikcie) vývoja testikulárnych funkcií. Muž môže mať po úspešnej asistovanej reprodukcii zdravé dieťa, pričom jeho semenníky sú rovnaké ako pred asistovanou reprodukciou.
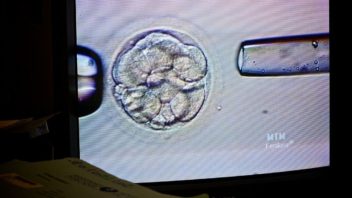
Najmodernejší analyzátor spermatozoidu – Sperm Quality Analyzer – Vision umožňuje páru prehliadnuť si spermie na obrazovke, spolu s ošetrujúcim lekárom zhodnotiť ich stavebný a funkčný stav a uložiť záznam v digitalizovanej podobe. Záznam je potom možné kedykoľvek porovnať s nálezom po liečbe. Nález si muž – budúci otec môže uchovať, pretože môže po určitom čase zatúžiť stať sa rodičom aj po druhýkrát.
Druhým dôležitým faktorom predikcie je hormonálne prostredie pacienta. Zvyčajné stanovenie hladín gonadotropínov, prolaktinémie a testosteronémie často nestačí. Treba zhodnotiť vzťahy hypotalamo-hypofyzárno-gonadálne (HHG os: medzimozog – podväzok mozgový – pohlavné žľazy), dať ich do korelácie s androgénnou nadobličkovou aktivitou, zhodnotiť pomer medzi väzbovými plazmatickými proteínmi (SHBG, albumín) a vzťahom testosterónu a estrogénov.
Antiandrogénna aktivita prolaktínu (na úrovni centrálneho nervového systému – CNS), progesterónu a kortizolu (na úrovni CNS a semenníkov) môže ukazovať na kauzálne riešiteľnú príčinu poruchy spermiogenézie i na možnosti aktuálnej prípravy k asistovanej koncepcii. Dynamické vyšetrenie HHG osi poskytnú LHRH (GnRH – Gonadotropine Releasing Hormon) test, tamoxifénový test a hCG (choriongonadotropínový) test. Morfologické pomery (stavbu) hypotalamu a hypofýzy najlepšie objasňuje magnetická nukleárna rezonancia.
Akékoľvek nálezy je nutné korelovať s vekom a klinickým stavom pacienta. Tu zohráva úlohu celý rad detekovateľných, predikatívnych faktorov (znaky celkovej andropénie – habitus, kožná adnexa, hypotrofia či hypoplázia testes, prostaty, semenných vačkov, disociácia epididymis od testis), ktoré vyžadujú detailnejšie prístrojové a laboratórne vyšetrenia.
Prediktívnu hodnotu v zmysle, „či sa pokúšať o asistovanú reprodukciu“, má genetické vyšetrenie, ktoré je dôležitou samostatnou kapitolou.
Príprava muža na asistovanú koncepciu
Ak je indikovaná asistovaná reprodukcia, je v záujme všetkých zúčastnených, aby bola pravdepodobnosť úspechu čo najväčšia. Čím zložitejší, dlhší a prácnejší postup, tým väčšie sklamanie v prípade, že nie je úspešný. Dôležitá je i ekonomická stránka.
Ak je zachovaná integrita HHF osi (os: medzimozog – podväzok mozgový – semenníky), napríklad u nonobštrukčnej azoospermie s andropéniou a s adekvátnou reakciou gonadotropínov (alebo FSH), usudzujeme aspoň o čiastočnom zachovaní fyziologickej regulácie tvorby spermií. Medikamentózny zásah do HHG osi je zvyčajne úspešný. Predpokladom na zlepšenie prietoku krvi semenníkmi a riešenie nedostatku testosterónu v tkanive semenníkov je dosiahnutie prietoku krvi semenníkmi s nízkym odporom tkaniva v oblasti tepien s normálnym žilovým odtokom pri funkčnom systéme žilových chlopní.
Leydigove bunky sú schopné produkovať dostatok testosterónu len pri dostatočnom prísune kyslíka, živín a neprítomnosti negatívnych faktorov vznikajúcich pri prerušovanom prietoku krvi. Hladina testosterónu v tkanive semenníkov je v periférnej krvi až stonásobne vyššia.
Podobne je ovplyvnený metabolizmus Sertoliho buniek, ktoré poskytujú „metabolický servis“ bunkovému radu spermiogenézy.
Objem tkaniva semenníka by mal byť aspoň 10 – 12 ccm. Ak je objem tkaniva menší než 6 ccm, pravdepodobnosť získania zárodočných buniek i pri mikrochirurgickom odbere výrazne klesá.
Negatívnym faktorom pri mikrochirurgickom odbere zárodočného tkaniva je u mužov s azoospermiou porušená integrita osi medzimozog – podväzok mozgový – semenníky. U azoospermie s normálnou priechodnosťou semenníkových ciest môžeme zistiť nedostatok testosterónu bez adekvátnej odpovede v oblasti tvorby hormónov podväzku mozgového (tvorbu spermií reguluje FSH = folikuly stimulačný hormón, tvorbu testosterónu LH – ICSH = luteotropné, intesticiálne bunky stimulujúce hormón).
Svoju úlohu tu zohráva inhibínový a aktivínový systém semenníkov (inhibín a aktivín sú informačné molekuly produkované bunkami semenníkov pre podväzok mozgový a medzimozog). Vyšetrenie hladín inhibínu B je však nákladné i v krajinách s kvalitným systémom financovania zdravotníctva. Z vlastných skúseností i z literárnych údajov vyplýva, že hodnotenie hladiny sérového FSH má určitú, hoci limitovanú prediktívnu hodnotu.
Ak je hladina FSH nižšia ako 20,3 IU/1 (to je medzi hornou hranicou normy a 20,3 IU/1), je možné očakávať lepší výsledok mikrochirurgického odberu (Tournaye 2001). Intratestikulárny deficit testosterónu je možné medikamentózne podstatne lepšie ovplyvniť pri zachovanej funkcii HHG osi. V opačnom prípade je to ťažké i pri dobrej testikulárnej hemoperfúzii.
Dostatočná mikrocirkulácia a nutrícia tkaniva testis je základným predpokladom úspechu prípravy. Cievne postihnutie môže byť vrodené – kongenitálne (vzácne artériovenózne malformácie), kongenitálne + získané (elastínová, kolagénna deficiencia žilovej steny + zvýšenie vnútrobrušného tlaku pri zdvíhaní bremien = varikokéla) či len získané (vaskulitídy, artériosklerotické postihnutie pri fajčení, poruchách metabolizmu cholesterolu a lipidov).
Podľa príčiny indikujeme terapiu, či už operačnú (mikrochirurgická extirpácia A-V malformácia, mikrochirurgická varikokélektómia), či medikamentóznu (endoteliálne aktívne látky, hemorheologiká, vazodilatancia, alfa-adrenergná venotonika). Na hodnotenie hemoperfúzie testes pred rozhodovaním o liečbe a asistovanej reprodukcii je dôležité dopllerovské vyšetrenie semenníkov a ich ciev. Výhodou tohto vyšetrenia je získanie množstva dôležitých informácií úplne bezbolestne a bez záťaže tkaniva.
Ovplyvnenie zachovanej HHG osi je možné na hypofyzárnej úrovni: stimulácia pomocou analóg GnRH, substitúciou hypofyzárnych hormónov či ich funkcií – FSH, hCG či pomocou rebound fenoménu vyšších dávok androgénov (prostredníctvom hypotalamu). Hypofýzu stimulujú blokátory estrogénových receptorov (clomiphen dihydrogéncitrát, tamoxifén), ktoré možno podávať perorálne. Substitučné dávky androgénov tu nie sú indikované, ich podávanie je kontraproduktívne – útlmom HHG osi môžu znižovať intratestikulárnu hladinu testosterónu.
Príprava môže významne zvýšiť úspešnosť operačného získania zárodočných buniek. Šetrné mikrochirurgické techniky „Sperm Retrival Techniques“ nahradili skôr užívané MESA („Microepididymal Sperm Aspiration“) a TESE („Testicular Sperm Extraction“). Ani kvalitná príprava a perfektne vykonaná operácia však nezaručujú stopercentný úspech.
H. Tournaye (2001) sa zaoberal získaním zárodočných buniek u mužov s azoospermiou. Okrem zaujímavého motta „azoospermia is not a diagnosis, azoospermia is a symptom“ priniesla jeho práca celý rad praktických informácií. Podľa vlastných skúseností (GEST, Centrum reprodukčnej medicíny, Praha 5) je nutné súhlasiť s jeho poňatím mikrochirurgického odberu zárodočného tkaniva z epididymis a testis „Sperm Recovery (Retrival) Technique – SRT“.
Tento postup je možné odporučiť:
- snažiť sa predpovedať úspešnosť odberu
- zabrániť poškodeniu semenníka odberom s následným zhoršením hormonálnej aktivity
- radšej zvoliť menej invazívnu aspiráciu z nadsemenníka než invazívnejší odber tkaniva z testis
- pri odbere tkaniva z testis voliť postup od menej invazívnych viacpočetných miniincízií s mikrodisekciou intralobulárne a až pri neúspechu invazívnejšiu cirkumferenciálnu incíziu tunica albuginea s mikrodisekciou translobulárnou (väčšie poškodenia ciev, ktoré prebiehajú v interlobulárnych septách)
- snažiť sa o kryoprezerváciu tkaniva testis
Tento prístup vyžaduje možnosti podrobnej predoperačnej diagnostiky a predoperačného embryologického hodnotenia vzoriek tekutiny z kanálov nadsemenníkov (aspirátu z epididymis) a tkaniva odobraného zo semenníkov. Dostatočné zväčšenie umožňuje veľmi dobrú diferenciáciu naplnených kanálikov epididymis vhodných k aspirácii. Množstvo aspirovanej tekutiny môže byť veľmi malé, preto i pri „neúspešnej“ aspirácii vyplachujeme ihlu kultivačným médiom, spermie sú totiž často zachytené až v tejto tekutine.
Ak nie sú podľa peroperačného embryologického vyšetrenia v aspiráte prítomné zárodočné bunky, pokračujeme incíziou tunica albuginea testis (steny semenníka). Incíziu vedieme podľa anatomického usporiadania tepien v interlobulárnych septách (priehradky medzi lalokmi), vždy pozdĺžne s ich priebehom, nikdy nie priečne na ich priebeh. Tepnové usporiadanie je možné ozrejmiť peroperačným dopplerovským vyšetrením (CFM = Color Flow Mapping).
Toto vyšetrenie zároveň podá informáciu o kvalite arteriálneho zásobenia určitého lobulu (laloku) tkaniva semenníka. Lepšia hemoperfúzia zvyšuje pravdepodobnosť úspechu pri odbere. Odber je predsa len niekedy hľadaním ihly v kope sena. Miniincíziu tunica albuginea o dĺžke 2 – 3 mm vykonávame hrotom kosákovitého skalpela na jedno použitie, a to pri dostatočnom zväčšení, ktoré umožňuje vyhnúť sa drobným tunikálnym vénam.
Tie majú pri častej poruche venóznej evakuácie tendenciu ku krvácaniu, čo výrazne zhoršuje prehľad vo veľmi malom operačnom poli. Zväčšenie musí byť volené racionálne, v rozmedzí ôsmich až dvadsiatich násobkov. Ak zväčšíme operačné pole veľkosti 5 x 5 mm cez celú obrazovku monitora, nie je jednoduché sa v ňom pohybovať. Operačným mikroskopom či kamerou nie je možné spáriť zárodočné bunky. Tie vyžadujú zväčšenie najmenej stonásobné (optimálne tristo- až päťstonásobné).
Pred odberom hodnotíme šírku, náplň, farbu testikulárnych kanálikov a podľa nálezu vyberáme vhodné segmenty k odberu tkaniva. Odoberáme časť subtunikálne uložených testikulárnych kanálikov, vzorku o veľkosti 2 x 2 – 2 x 3 mm. Ak nie sú vo vzorke prítomné zárodočné bunky alebo nie sú v dostatočnom počte a kvalite, môžeme mikrodisekciou odobrať z tej istej incízie druhú, hlbšiu vzorku, prípadne podľa volumu testis i vzorku tretiu.
Vzorky z väčšej hĺbky sú vždy menšie. Pri mikrodisekcii dbáme na to, aby sme nespôsobili krvácanie. Prípadné krvácanie zastavíme až po ukončení odberu z miniincízie pomocou termokoagulačnej či bipolárnej sondy (pinzety) s veľmi jemných hrotom. Incíziu uzatvárame atraumatickým plne resorbovateľným šijacím materiálom Vicryl 4/0 (USA) ihlou využívanou k očným operáciám.
Ak nie sú vo vzorkách z jednej incízie prítomné zárodočné bunky, vykonávame ďalšiu incíziu („Multiple Biopsy Technique“), znova s peroperačnou spätnou väzbou na embryológa. Na jednom semenníku vykonávame podľa objemu testis maximálne päť až sedem miniincízií s odberom maximálne pätnástich vzoriek o veľkosti 2 x 3 až 1 x 1mm. Vzorky by mali mať hmotnosť do 15 mg tkaniva (bežné bioptické vzorky sú o hmotnosti okolo 500 mg).
Nevýhodou je, že takéto malé vzorky sa zle kryokonzervujú (zmrazujú), preto po „mapovaní“ tkaniva semenníka môžeme pri dostatočnom objemu semenníka ku kryoprezervácii zvoliť vzorku s väčším objemom, maximálne do veľkosti 3 x 5 mm. Vzorku je možné odobrať i z trojmilimetrovej incízie po mikrodisekcii so šetrným „vytiahnutím“ tkaniva spod tunica albuginea.
Po ukončení odberu tkaniva kontrolujeme neprítomnosť krvácania z incízií s opakovaným opláchnutím steny semenníka (tuniky albuginey) fyziologickým roztokom, starostlivo rekonštruujeme tunica vaginalis testis, suturu (steh) obalov vykonávame Vicrylom 3/0 – 4/0, suturu kože Vicrylom 3/0 rapid s atraumatickými ihlami. Výkon by mal byť „patient friendly“, teda nebolestivý v celkovej anestézii, pokiaľ možno bez nutnosti hospitalizácie, so zvládnutím pooperačnej bolesti vhodnými analgetikami a s prevenciou proti infekcii. Vykonávame ju preto v antibiotickej clone.
Operačná rana na miešku je krytá sterilným obväzom počas dvadsiatich štyroch hodín, potom volíme otvorené ošetrenie s tým, že pacient sa môže sprchovať a do slipov si vkladá sterilný štvorec gázy. Pooperačnú analgézu potrebuje väčšina pacientov len prvú noc po operácii (napríklad Tramadol kvapky). Operácia je subjektívne menej nepríjemná ako napríklad stomatologické ošetrenie zubného kazu. Týmto postupom boli získané spermie u šesťdesiatich šiestich percent operovaných mužov (Poláková et al. 2003).
Z andrologického hľadiska existuje ešte jeden dôležitý rozmer mužskej infertility. Ide o hormonálny stav mužského organizmu.
„Androcheck“ koncepcia
Koncepcia vychádza zo znalosti účinkov androgénov na cieľové tkanivá a orgány. Je známa nutnosť dostatočných hladín androgénov pre reprodukčné a sexuálne funkcie (spermiogenézia, erekcia, ejakulácia). Androgénmi je však ovplyvnený metabolizmus proteínov v celom organizme. Proteosyntéza a obnova tkanív pri dlhodobom nedostatku androgénov môže byť nedostatočná.
Problémy sa týkajú svalového tkaniva, kostného tkaniva, produkcie imunoglobulínov, erythropoetínu, centrálnej i periférnej nervovej sústavy, funkcií kardiovaskulárneho systému a metabolizmu lipoproteínov. Následky plynúce z nedostatku testosterónu sú podobné klimakterickým ťažkostiam u žien. Osteoporóza, zníženie pohyblivosti pri svalovej ochabnutosti, relatívna imunodeficiencia, zhoršenie kognitívnych schopností CNS (pamäť, učenie), akcelerácia artériosklerózy, psychické ťažkosti (depresie) a sexuálna dysfunkcia sa týkajú všetkých mužov s poruchou hormonálnej funkcie semenníkov. Perspektíva starnutia je nevyhnutná.
U muža je fyziologicky najvyššia hladina androgénov medzi dvadsiatym štvrtým až tridsiatym rokom života. Potom dochádza fyziologicky k pomalému poklesu s veľkými interindividuálnymi variáciami. Vo veku šesťdesiatich piatich rokov je hladina testosterónu v porovnaní s dvadsiatym piatym rokom života približne polovičná. Ak má pacient testosteronémiu nižšiu už medzi dvadsiatym a tridsiatym rokom života, môže pokles sledujúci vek pacienta dosiahnuť výraznú andropéniu v relatívne mladom veku (medzi 35. – 45. rokom života), a to so všetkými negatívnymi následkami.
Znížená hladina androgénov je v príčinnej súvislosti s akceleráciou biologického starnutia so všetkými organickými ochoreniami a znížením psychickej kondície. Na tieto problémy je v prípade infertilných mužov nutné myslieť už v mladom veku. Väčšina z nich je vo veku medzi dvadsiatym a tridsiatym piatym rokom života, teda v období, keď by mali mať hladiny androgénov najvyššie. Znížené sérové hladiny androgénov, hormonálna dysbalancia tvorby androgénov sú detekovateľné u väčšiny infertilných mužov.
Nálezy andropénie sú časté i v prípade obštrukčného postihnutia semenníkových ciest. Pozápalové fibroproliferatívne zmeny postihujú okrem semenníkových ciest aj cievny systém semenníkov.
Aj u vrodeného postihnutia je pri chýbajúcom chámovode (vas deferens) možné postrehnúť zníženie tepnového prietoku semenníka v prípade, že chýba perfúzny gradient chýbajúcej tepny chámovodu.
Znížená hladina hormónov v mladom veku nemusí byť subjektívne pociťovaná, pretože nebolí, rovnako ako ani porucha spermiogenézie. Po uspokojení túžby po dieťati pacienti často na ďalšiu diagnostiku a liečbu zabúdajú. Ak ich postihnú ťažkosti súvisiace s andropéniou v staršom veku, nie sú už ošetrení na pracoviskách asistovanej reprodukcie.
Navštevujú ordinácie urológov, sexuológov, neurológov, kardiológov a andrológov. Pracovisku asistovanej reprodukcie tak chýba spätná väzba.
Lekárom uvedených odborností chýbajú niekedy informácie, niekedy čas, energia a motivácia hľadať nové asociácie polymorfných ťažkostí svojich pacientov. Na hormonálne problémy preto myslí častejšie endokrinológ a andrológ.
Efekty liečby napríklad cievneho ochorenia semenníkov sú v piatej a v šiestej dekáde života podstatne slabšie ako v dekáde druhej či tretej. Môžeme sa stretnúť aj s tým, že gynekológ infertilnému pacientovi vyhovorí naplánovanú varikokélektómiu, lebo z jeho hľadiska sa efekt dostavuje až po uplynutí príliš dlhého času.
Androcheck koncepcia spočíva najmä v hľadaní súvislostí medzi hormonálnym stavom muža a liečbou (prevenciou) ochorenia tkaniva a orgánov, ktoré sú ovplyvňované androgénmi.